バッグバルブマスクについて
バッグバルブマスク(Bag valve mask, BVM)は、口腔よりマスクにて用手換気を行うための医療機器である。構造の違いによってアンビューバックとジャクソンリースに分かれる。
アンビューバック
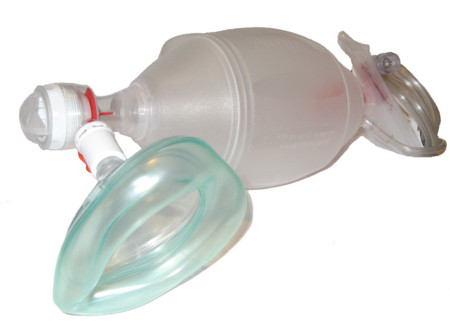
アンビューバッグ(Anbu bag)は、バッグに送気逆流弁と自動膨張機能を設置したBVMで、元々はドイツのAnbu社のオリジナル製品。 1953年にドイツ人のオルガー・ヘッセ博士とデンマークの麻酔科医ヘニング・ルーベンによって開発された。救急現場の第一線で幅広く用いられる。
現在、複数の会社から製造販売されているが、Anbu社の製品が有名なため世界的にアンビューバッグの名が一般化している。
アンビューではガス源は不要で、酸素流量は0〜10L/min、バッグの拡張は自動、CO2再呼吸はなく、高濃度の酸素吸入にはリザーバーを要し、肺の状態把握や加圧圧力はわかりにくい、構造は一方方向弁をもち、価格は高価といえます。機種により圧力計やPEEP弁が付いているものがあります。
CO2ナルコーシス
CO2ナルコーシス(高炭酸ガス血症)とは
概要
CO2が過剰に蓄積し、高炭酸血症を来たすと、CO2の血管拡張作用(頭蓋内圧亢進作用)によって頭痛が生じるとともに、中枢神経抑制作用を来たす。同時に呼吸中枢も抑制されるのでますますCO2が蓄積するという悪循環に陥る。
原因
臨床上でもっとも注意しなければならない点は、慢性のII型呼吸不全に対して不用意に高濃度O2を投与すると、本症を誘発することである。つまり、II型呼吸不全が慢性的に持続すると、呼吸中枢は高濃度のCO2にすっかり馴れてしまい、もはや何の刺激も感じなくなる。この状況で呼吸中枢を刺激しているのは、O2の不足(PaO2の低下)のみである。したがって、突然体内に高濃度のO2が入ってくると、その刺激が奪われてしまい、自発呼吸が停止してしまう。すると治療のために投与したO2のせいでどんどんとCO2が蓄積し、CO2ナルコーシスに陥ってしまう。
- 通常は CO2刺激(高CO2)で呼吸中枢が促進される。
- COPDでは O2刺激(低O2) で呼吸中枢が促進される→高流量O2にて呼吸停止。
症状
高炭酸血症では頭痛、振戦、痙攣、傾眠がおこる。特に発汗は著明で、体温に関係なく見られる。頭痛、振戦は早期症状として重要である。頭痛は低酸素血症や高炭酸ガス血症による脳血流増加に基づく脳圧亢進によるものと考えられている。
また、呼吸不全には電解質異常を伴うことが多く、それによる中枢神経症状が出現する。呼吸性アシドーシスでは高K血症を伴うことが多いが、この状態が長く続くと、尿中にKが排出され、逆に低K血症になる。高K血症では、知覚、運動障害が徐々に出現する。意識、精神障害は通常少ない。その他、しびれ感、灼熱感などの異常感覚と筋脱力感、筋痙攣をみる。低K血症ではときに無関心、無気力などをみる。血清Naが120mEq/l以下になると倦怠感、傾眠、異常言動や錯乱などが出現する。
診断
上記症状、病歴、動脈血ガス分析、胸郭X線写真などにより行う。確定診断には動脈血ガス分析が必須であり、通常PaCO2>80Torr、 pH<7.30ではCO2ナルコーシスを合併している可能性が高い。しかしながら、慢性閉塞性肺疾患の患者ではこれより高くても意識障害が出ない場合がある。また、中枢神経疾患(脳血管障害、脳髄膜炎)、代謝性脳症(糖尿病性昏睡、肝性脳症、尿毒症性昏睡)、薬物中毒などとの鑑別が必要である。
治療方針
- 低濃度・低流量酸素投与
慢性呼吸不全患者では、日常的に高炭酸ガス血症になっているため、呼吸中枢の二酸化炭素に対する反応が低下している。肺疾患を有する場合、ベンチュリー・マスクで24〜28%O2を吸入、もしくは鼻カニューラでO2を 0.5〜1.0L/分で吸入する。目標のPO2は50〜60Torr、パルスオキシメーターでSpO2を90%、PCO2を75Torr以下を目標とし、意識状態を頻回に確認する。
- 人工呼吸管理
- 非侵襲的陽圧換気(NPPV:noninvasive positive pressure ventilation)
- 人工呼吸器管理
http://www13.plala.or.jp/thoraco/homework/shukudai25.html
http://nayami.tabine.net/ns/000034.html
BIPAPについて
biPAPは、bilevel Positive Airway Pressureの略で、もともとは侵襲的、非侵襲的に関係なく、その換気モードを意味する言葉でしたが、フジ・レスピロニクス社の BiPAP Visionが有名になり、非侵襲的の二相式ベンチレーターのことをさす言葉として一般に使用されています。

フジ・レスピロニクス http://www.fuji-respironics.com/product/hospital.html
IPPVとBIPAP
挿管されて人工呼吸器に接続されたばかりの患者においては、従来はIPPVによる換気が選択されることが多かった。このモードは呼吸のすべてが人工呼吸器による機械換気で、患者の自発呼吸はすべて制限される。このため、筋弛緩薬や大量の鎮静剤は不可欠になる。一方、BIPAPでもIPPVと同じような圧波形を供給することはできるが、患者は機械換気の最中であっても、どのタイミングでも自分の呼吸を行うことができる(機械換気が吸気中であっても、患者が息を吐きたいと思えば吐ける)ので、筋弛緩薬や鎮静剤の量を減らすことができる。さらに、機械換気中であっても患者自身の呼吸量が加わるために換気量をその分減らすことができ、結果としてピーク気道内圧をより少なくすることもできる。
PCVとBIPAP
気道内圧波形を見比べただけでは、PCVとBIPAPは区別がつかないぐらいによく似ている。どちらも圧制御型の換気様式で、患者の吸気に同調して気道内に陽圧をかけ、それを設定された時間だけ続けようとする。

この両者でもっとも大きな違いは呼気弁の作動のしかたにある。PCVの場合、患者の吸気中は呼気弁は閉じている。このため患者が息を吐きたくなっても、設定した時間が来ないと呼気弁は開かず、この間は非常に苦しくなってしまう。BIPAPは、患者の吸気時間中であっても吸気弁を閉じることはせず、その開き具合を持続的に調節している。このため患者が息を吐きたくなった場合でもスムーズに呼吸ができ、その間も気道内圧は設定した値に保たれる。
プレッシャーサポートとBIPAP
患者にとって楽な呼吸を目指したモードとして、PSVとBIPAPとはよく比べられる。PSVは患者の吸気と呼気とをすべて患者のトリガーによって行うため、患者は非常に楽に呼吸できる。しかし、人工呼吸器のトリガーには限界があり、頻呼吸になればなるほど呼吸器の応答は悪く、患者の呼吸困難は増し、また換気の効率も悪くなる。
BIPAPもまた、患者の吸気に合わせて気道内圧を上げ、患者の呼気にあわせて気道内圧を下げる。しかし、気道内圧の変化は原則として設定した時間以内には行われないので、患者が頻呼吸になっても呼吸器の応答が保たれる。また、一定時間は患者の気道内圧は高い圧に保たれるので、品呼吸による換気効率の悪化が生じにくく、また自発換気を残したまま最低分時換気量を調節することができる。
biPAPの設定方法
挿管直後は、従来ならばIPPVやSIMVのモードが用いられる時期であるが、こうしたモードをBIPAPで代替することが可能である。従来のモードともっとも異なっているのが換気時間の設定で、従来の機械換気ではI/E比と換気回数を指定し、吸気時間と呼気時間を間接的に決定していたが、 BIPAPではこの2つの時間を独立して設定することができ、これらの時間の設定の結果I/E比や換気回数が決定する。挿管直後の急性期であっても、 BIPAPモードは患者の自発換気を消さないため、呼吸器の設定する換気回数やI/E比はあまり意味をもたなくなる。
また、従来型の機械換気であれば1回換気量を設定し、患者の気道内圧をモニターしていたが、BIPAPモードでは逆に気道内圧を設定し、患者の分時換気量をモニターすることになる。
具体的な設定としては以下のとおり。
1. 通常の呼吸不全の患者でのPEEP圧と同じ圧に、低いPEEP圧を設定する。
2. それよりも12-15cmH2O程度高い圧に、高いPEEP圧を設定(1回換気量を見ながら調節)する。
3. 高いPEEP圧の時間は1.5-2.5秒、低いPEEP圧の時間は3.5-2.5秒程度から開始し調節する。
4. 酸素化が悪ければ高いPEEP圧の時間を延長し、CO2の貯留があるようならそれぞれの時間を短く調節して換気回数を増加させる。

BIPAPのウィーニング
BIPAPモードは、ウィーニング中も同じモードを継続して使用できる。方法は以下のとおり。
1. 状態が落ち着き、FiO2を50%以下まで下げられたらウィーニング開始。
2. まずは高いPEEP時間を徐々に減らし、I/E比を1:1から1:3程度まで徐々に増加させる。
3. この間、患者の吸気、呼気にあわせて機械がタイミングを変更するので同調は気にしなくても大丈夫。I/E比を調節していくと、そのうちに作動はプレッシャーサポート換気とまったく同じになる。
4. 最後に高いほうのPEEP圧を徐々に減少していき、高いPEEP圧と低いPEEP圧が同じになると、CPAPと同じ動作波形が得られる。
5. これで問題なければ抜管を考慮する。
NPPVのbiPAP
NIPネーザルにおいては、
S: 自発呼吸に同調して、IPAP(吸気圧)とEPAP(呼気圧)を切り替えます。
T: 呼吸数と吸気時間にあわせて、圧が切り替わります。
S/T: Sモードに加え、一定時間自発呼吸が無い場合に吸気圧になります(バックアップ機能)。
CPAP: 吸気圧を連続送気します。
の4モードがあります。
コピペ元
エビタのBIPAPモード - レジデント初期研修用資料(旧)
http://medt00lz.s59.xrea.com/blog/archives/2004/11/bipap.html
http://medt00lz.s59.xrea.com/blog/archives/2004/11/bipap-2.html
VAPについて
VAP 人工呼吸器関連肺炎 ventilator-associated pneumonia
VAPを予防するには、口腔ケア時にオーラルバランス(ジェル状口腔湿潤剤)を使用する/呼吸器の回路交換をむやみに行わない/鎮静をかけすぎない/早期抜管を目指すことが有効。
http://pulmonary.exblog.jp/9859662/
http://www.h7.dion.ne.jp/~oka-shop/sub43.htm
またVAPを発症したら適切な抗菌薬の使用を行い、最初は広域のスペクトルの抗菌薬を使用し、徐々にde-escalationしていく。
VILIあるいはVALI 人工呼吸による肺損傷(Ventilator-induced(associated)lung injury
原因はVolutrauma(容量損傷)/atelectrauma(気道の周期的な虚脱)/Barotrauma(圧損傷)
- Volutrauma(容量損傷)
ARDS患者の場合、患者の肺のCTを撮ってみると肺は以下の3つの状態が混在していることが分かっている。
完全に虚脱し呼吸に参加していない肺胞/吸気時には空気が入るが呼気時に虚脱する肺胞/正常な換気を行っている肺胞
※このため、ARDSの患者の場合は正常な人に比べて換気している肺胞の数が少なく、たとえ常識的な1回換気量で換気を行っていたとしても、患者に残っている正常な肺胞には過大な1回換気量になってしまう。
- 気道の周期的な虚脱
ARDSで病的になった肺胞の一部は、換気にあわせて開放した状態と虚脱した状態とをいったり来たりする。この状態により生じる肺の損傷は atelectraumaと呼ばれている。
この、周期的に生じる気道の虚脱、開放は肺胞にダメージを与える。この運動により、肺胞内のサーファクタントは気管側に流出してしまい、虚脱した肺胞を再び開放するためにかかる圧力は肺胞の内皮細胞を障害する。
- Barotrauma(圧損傷)
Volutraumaの考え方以前に主流だったのが、気道内圧が高いこと自体が肺に障害を与えるという考え方である。
肺に過大な圧力を与えると肺の内皮細胞は障害されるが、この働きが病的な肺でどれだけ肺障害の成立に関与しているのかはまだ議論がある。
原理的には、Barotraumaは1回高い気道内圧で換気しただけでも生じうる。
- 炎症性サイトカインの増加
ARDSを生じた患者の多くで多臓器不全を生じるが、この原因の一つが人工呼吸器であるという考え方がある。最近の動物実験からは、人工換気により以下の2つの状態が引き起こされると考えられている。
炎症性サイトカインの増加/肺を通じた細菌の進入
ARDSの患者には多臓器不全が合併することが多いが、これは多臓器不全に伴ってARDSを生じるのではなく、 ARDSに陥った肺、あるいは人工呼吸器による肺障害自体が多臓器不全を引き起こす引き金になるという考え方がある。
ARDSやALIの状態になった肺には、好中球をはじめとした炎症細胞が多数浸潤している。このため、肺を通過した血液にはこうした細胞から分泌された炎症性サイトカインが多量に含まれ、これが多臓器不全を引き起こす原因の一つになっていると考えられている。
Ventilator associated lung injury - レジデント初期研修用資料(旧)
http://medt00lz.s59.xrea.com/blog/archives/2004/11/ventilator-asso.html
サーファクタント欠乏による無気肺への人工換気による肺損傷(athelectrauma, volutrauma)と、酸素毒性
APRVについて
YouTube - APRVとは:APRVの基本事項
APRV(Airway Pressure Reliese ventilation)

高いCPAP圧を用いると酸素化能の改善が期待でき、また、呼気解放により換気補助(CO2の排出)が期待できる。しかし、CPAP期間中に換気抑制を生じる欠点もある。したがって、圧差を多くしても、一概に換気補助が増加するとは限らない。いづれにせよ、自発呼吸の存在を前提条件であり、また、換気補助能力に限界がある点が適応上の制約である。
APRVについて - 人工呼吸管理に関するブログ - Yahoo!ブログ
http://blogs.yahoo.co.jp/rikimaru1979/8431419.htmlARDS(呼吸不全の最重症タイプ - 心不全による肺水腫以外の呼吸不全で、PF比:PaO2÷FiO2が200以下のもの)において、通常のCPAPでは自発呼吸を残した呼吸管理を行うことはなかなか困難です。パーミッシブ・ハイパーカプネア(こんだけ重症の呼吸不全なんだから、二酸化炭素の貯留はある程度は大目に見ようよっていう考え方)にならざるを得ないこともしばしばです。
(中略)
ARDSであれば驚きの20-30cmH2O程度のPEEPをかけます。この高い気道内圧下で自発呼吸をさせます。イメージは簡単だと思いますが、無気肺でつぶれてしまった肺胞を高い圧をかけて広げてやる感じです。肺胞を開いたopen lungの状態を作って、その上で(最も人工呼吸器による肺障害を少なくできる)自発呼吸をさせます。…でも、はじめから高いPEEPがかかってますから、ある程度肺が膨らんだ状態からの自発呼吸になってしまいますよね。この減少した換気量を補うために、リリースと呼ばれる喚起補助を行います。リリースですが、高いPEEPから一気に0cmH2Oまで圧を開放してやります。一気に圧が解放(呼気にあたる)されますから、このときCO2がはけます。今までの換気法では、圧をかけて(タイダルを吸わせて)喚起補助をしてましたよね。ここが大きな違いです。画期的!!!
でも、圧が0cmH2Oになるってことは、膨らんでた肺胞が虚脱してしまいますよね。(圧をかけて膨らませてた風船が、圧解除でつぶれてしまう。)で、このリリースですが、ごく短時間(通常0.4-0.6秒以内)で終了して、高い圧に戻してやるため、内因性のPEEP(風船は空気の出口がせまいため、空気が出て行くときに内側から圧がかかります)がかかったまま、肺胞が虚脱する前に呼気が終了します。
つまり、APRVは
①ARDSのようなCO2がたまりやすい病態でも自発呼吸が温存でき、
②高圧相は高い気道内圧で肺胞を開き、リリースのときは内因性のPEEPによって肺胞が虚脱しない換気法なんです。
まとめ:HighPEEPは20-30cmH20、lowPEEPは0chH20、Tlow(リリース時間)は0.4-0.6sec(内因性PEEPにて再虚脱を防止)
APRVの基礎と臨床 - RST*Blog
http://icuweb.biz/blog/archives/2008/01/27-004238.php注意点はAPRVを用いると血液ガスが良くなるけれど,それに騙されてはいけないということ。レントゲン所見と血液ガスは必ずしも一致しないため,血液ガスが良くなったからと言ってレントゲン所見を確認せずに抜管すると痛い目にあうと言われていました。
(中略)
Phighの設定は重要で,肺胞の解放圧+αへの対抗圧を推定,わからないときは25cmH2Oから開始してみる。リリース時には圧基線を0にせず,AutoPEEPを作る。P Highを下げたら必ずT Highを延ばす。T lowは圧解放時の流量波形とAutoPEEPのかかり具合から設定し,通常0.4〜0.8秒程度。ちなみに,APRVの再開通効果は,8時間後から酸素化改善効果をみせはじめ,16時間以降はさらなる効果は見られないそうです。
離脱については,P Highの下げ幅は1日に2,3程度にすること。Pを下げるよりも早くTを延ばすのが大切なのだそうです。
